腎癌
腎細胞癌(腎癌)は成人の癌の約3%を占め、男性は女性比べて2-3倍多く、50歳代後半から増加し、70歳代前半にピークになると言われています。近年では20~30代の発症報告も増えてきており、腎癌数および死亡数は増加傾向にあります。腎癌も他の癌と同様に決して治らない病気ではありません。早期に発見された腎癌は予後良好であるのに対して、進行例では予後不良であるため、早期発見が重要と言えます。最近では分子標的薬や免疫チェックポイント阻害薬という新しい薬も登場し、進行例おける予後は改善傾向にあります。
病期分類
| 病期Ⅰ | 7cm以下の腫瘍が腎に限局[T1]し、所属リンパ節や他臓器転移を認めない。 |
|---|---|
| 病期Ⅱ | 7cmを超える腫瘍が腎に限局[T2]し、所属リンパ節や他臓器転移を認めない。 |
| 病期Ⅲ | 腎周囲脂肪または主静脈(腎静脈や下大静脈)に進展するが、同側副腎への進展がなく、Gerota筋膜を超えない腫瘍[T3]。または、T1~2の腫瘍で、他臓器に転移がなく、所属リンパ節に1個の転移を認める。 |
| 病期Ⅳ | Gerota筋膜を超えて浸潤する腫瘍(同側副腎への浸潤を含む)[T4]。または、T1~3の腫瘍で、他臓器に転移があるか、所属リンパ節に2個以上の転移を認める。 |
症状
小さな腎癌ではほとんどが無症状ですが、癌が大きくなるほど症状が強くなり、以下のような症状を呈することがあります。
| 全身症状 | 発熱、倦怠感、体重減少 など |
|---|---|
| 原発巣による症状 | 血尿、側腹部痛、腫瘤蝕知 <古典的3主徴> など |
| 転移巣による症状 | 血痰、腰痛 など |
近年、健康診断や他の疾患の精査(エコーやCT検査)で偶然発見される、症状のない腎癌(偶発癌)が増加傾向にあり、全体の70%以上とされています。偶発癌で発見されて治療を受けた場合、上記のような症状が出現して治療を受けた場合と比べ、治療成績が良いというデータがあります。
診断
腎癌では、血液検査や尿検査で診断できる有用な腫瘍マーカーは今のところありません。
エコー、CTスキャン、MRIなどの画像検査によって診断の中心となります。しかし、画像検査で良性・悪性の確定はできないため、術後に良性腫瘍と診断される場合も約10%あります。まれに背部からエコーやCTスキャン下に針を穿刺して組織を採取する検査(生検)を行って診断する場合があります。
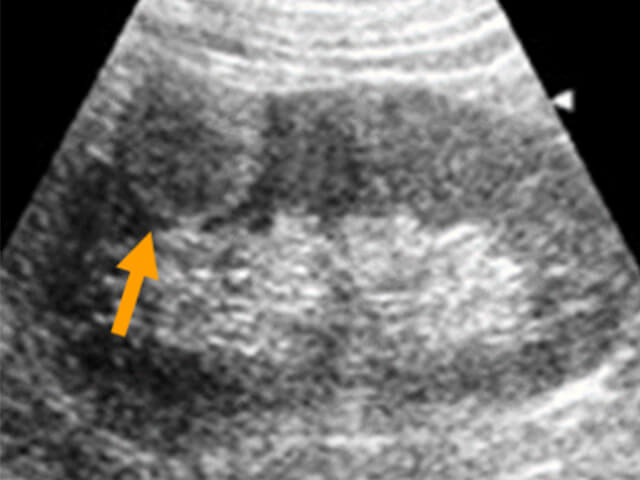
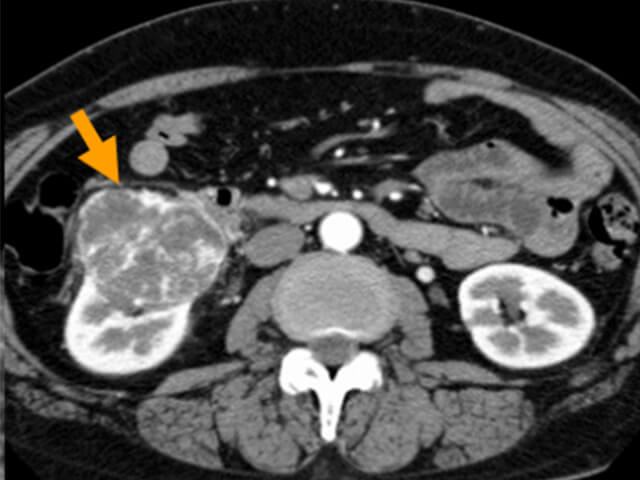
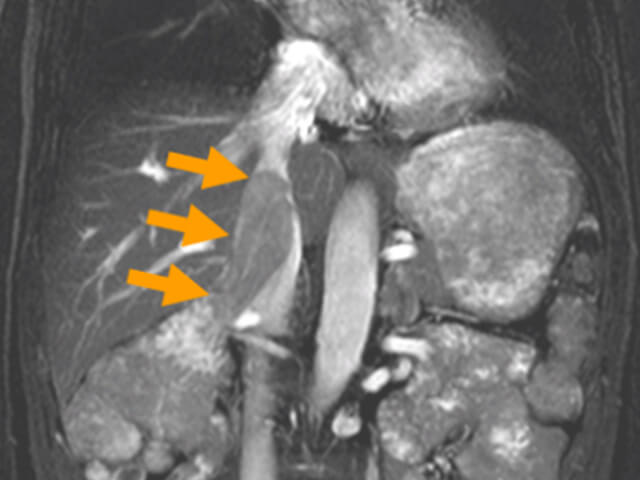
治療
1.手術療法
一般的には病期Ⅰ~Ⅲに対して行います。しかし病期Ⅳであっても、切除が可能であれば癌とともに腎臓を摘除する場合もあります。
Ⅰ.腎部分切除術
癌が小さい場合(一般的には4cm以下)に適応となります。癌のみを切除し、腎臓は温存する手術です。腎摘除術に比べ、制癌効果は同等であり、術後の腎機能温存や心血管イベント減少の点で有用とされています。腹腔鏡で行う場合と、開腹手術で行う場合がありますが、術式をどちらにするかはその症例ごとに検討します。当科では、ロボット支援腹腔鏡下腎部分切除術を積極的に行っています。低侵襲かつ正確性の高い術式です。これについては「ロボット支援腎部分切除術」の項をご参照下さい。
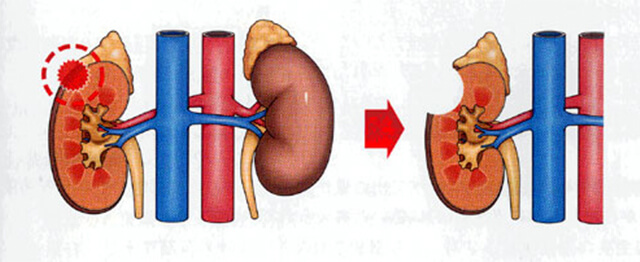
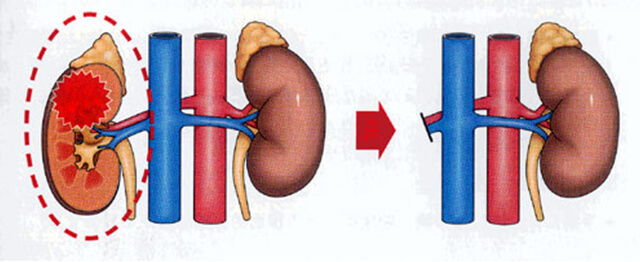
Ⅱ.腎摘除術
癌が比較的大きい場合(一般的には4cm以上)に適応となります。癌のある腎臓を腎周囲脂肪と一塊にして摘除します。場合によっては副腎やリンパ節も切除します。最近では腹腔鏡による手術を行う割合が高くなっており、その場合手術の傷も小さく、術後の回復も早く、傷の痛みも少ない特徴があります。
2.薬物療法
転移を伴う進行性腎癌に対して行う全身治療です。腎癌は抗癌剤や放射線が効きにくいという特徴があるため、以前では、進行例の予後は不良とされていました。近年では、新しい薬剤が次々と認可され、進行例の予後は改善傾向にあります。
Ⅰ.サイトカイン療法
免疫担当細胞(リンパ球など)を刺激して、癌細胞の排除を促進する治療法です。インターフェロンという注射を、連日~週3回程度の頻度で筋肉注射します。またインターロイキンという薬を、連日~週2回程度点滴する治療法もあります。サイトカイン療法は、以前は薬物療法の中心でしたが、その奏効率は10%程度で、後述する薬粒療法の登場により、現在ではほとんど使用されなくなっています。
Ⅱ.分子標的治療
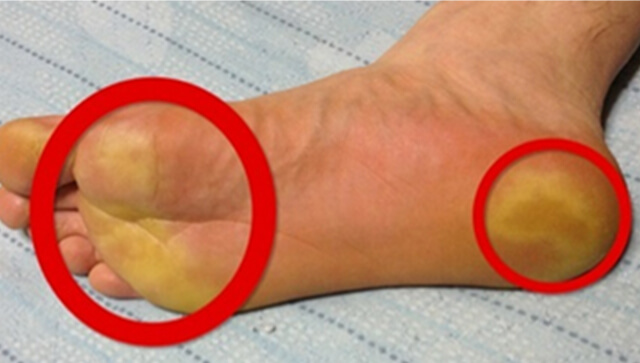
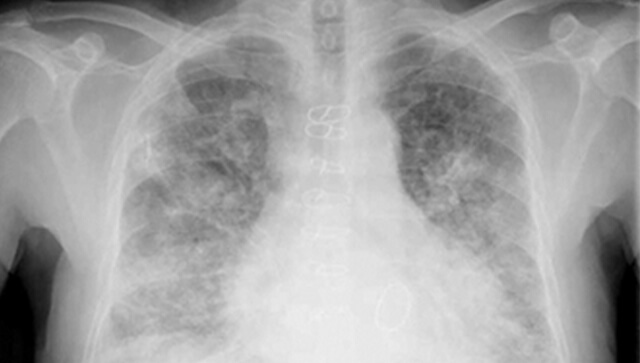
腎癌の増殖に関連する分子を標的とした治療薬で、2008年以降に登場した薬剤です。腎癌の増殖に際して細胞内で交わされるシグナル伝達(信号の受け渡し)を標的にして、増殖を抑制します。現在、日本では7種類の分子標的薬が認可されています。分子標的薬には、手足症候群、高血圧、甲状腺機能低下症、下痢、間質性肺炎、高血糖などの特有の副作用がありますが、これらの中には治療効果を反映するものもあります。
Ⅲ.免疫チェックポイント阻害薬
免疫担当細胞の表面には「免疫チェックポイント分子」と呼ばれる、免疫機構にブレーキをかけるスイッチのような分子が発現しています。本来は、免疫が過剰になり過ぎて自分自身を攻撃しないように備わっているスイッチです。癌細胞は増殖する過程でこのスイッチを獲得して、免疫機構から逃れるようになります(免疫逃避)。免疫チェックポイント阻害薬は、このスイッチに蓋をして免疫機構にブレーキをかけさせないようにする薬剤で、2016年に認可されました。もともと生体に備わった免疫機構を利用するため、一般的な抗癌剤と比較して副作用の頻度が少ないのが利点ですが、免疫が過剰となって自分自身を攻撃してしまう副作用(免疫関連有害事象)が一定の頻度で見られるという欠点もあります。免疫関連有害事象は時に重篤となり、ステロイド治療が必要となることもあります。効果に関しては、約30%の人で長期間の腫瘍縮小が見られる一方で、約40%の人では効果が得られないといった一面があります。しかし、どのような人で効果が得られやすいかということは、今のところはっきりわかっていません。2018年以降では、免疫チェックポイント阻害薬と分子標的薬を併用した、さらに強力な薬物療法も使用可能となっています。
<免疫関連有害事象> … 頻度は比較的少ないが多彩な症状
脳炎、下垂体機能低下、甲状腺機能低下、肝機能障害 、Ⅰ型糖尿病、腎障害、大腸炎、静脈血栓、間質性肺炎、重症筋無力症、皮膚障害 etc
3.その他の治療法
Ⅰ.ラジオ波焼灼術
- 腫瘍にラジオ波を通電し、腫瘍組織の温度を上げて焼灼する治療
- 手術より低侵襲で、何度でも繰り返し治療ができるのが利点
- 局所再発率 3~7 %
Ⅱ.凍結療法(クライオアブレーション)
- -100℃以下となるプローブで、腫瘍やその周囲を凍結させる治療
- 手術より低侵襲で、何度でも繰り返し治療ができるのが利点
- 局所再発率 6~13 %
Ⅲ.放射線治療
- 腎癌の原発巣の治療としては、ほとんど使用されない
- 脳転移、骨転移での有効性が高い
- 放射線特有の有害事象がある(皮膚障害、肺障害、下痢、頭痛 etc)
