
初期胚におけるエピジェネティックな遺伝子制御過程の追跡とその応用 哺乳動物の発生は、生殖細胞である卵子と精子の受精から始まります。受精卵では遺伝子発現が時間的空間的に調節されることで、細胞分裂が開始し、体を作る準備が進められます。近年、遺伝子発現の制御にはゲノム配列のみならずエピジェネティックな修飾も重要であることが明らかになってきました。私たちは主にマウス初期胚におけるエピジェネティックな遺伝子制御機構に着目して研究しています。 1.雌におけるX染色体不活性化の可視化とメカニズムの解明 哺乳類では、XXとXYという性染色体の組み合わせにより雌と雄を表していま 2.雌雄ゲノムの脱メチル化制御特性の解析 卵子と精子は基本的に同じ遺伝子を持ちますが、受精卵で核移植の実験を行うと、雌だけのゲノムでも雄だけのゲノムでも胚発生が停止することが知られています。この原因としては、雌雄のゲノムがそれぞれ異なるエピジェネティックな修飾を受けて、互いのゲノムの機能に違いを生じさせているためだと考えられています。このような違いはゲノムインプリンティングと呼ばれており、配偶子が作られる過程で付加されるDNAのメチル化の違いによると言われています。私たちは、配偶子が作られた後の受精卵でも雌雄のゲノム機能の差異が確立されることに着目し、メチル化した外来性のDNAとマイクロインジェクション技術を利用しながら、雌雄ゲノムの違いを評価したり、その違いが確立される機構を解析しています。 |
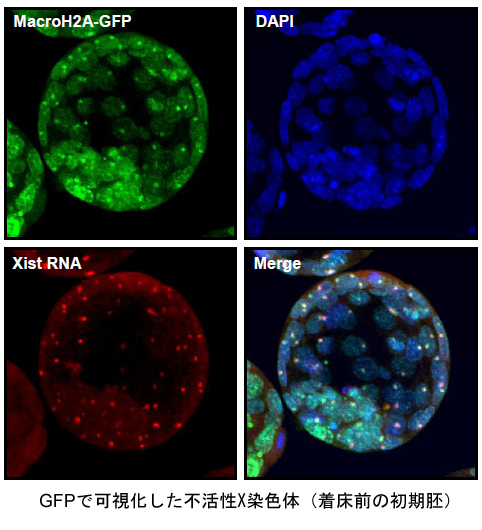 す。そのため、雌では
す。そのため、雌では